莽草酸通路是合成分支酸的唯一途径。团队研究人员发现,该通路很可能在细菌和古菌还没有分化之前就已存在于它们的共同祖先中。所有的酶组合在一起构成完整的莽草酸通路的过程也可以很好地通过拼凑假说(patchwork)来解释。随着细菌与古菌的分歧,莽草酸通路出现了变形。负责通路头尾生化反应的酶在进化过程中出现了同源但具有明显系统发育距离的亚家族,同时横向基因转移也在该通路的进化过程中发挥着重要作用。该成果发表在《分子系统发育与进化》(Molecular Phylogenetics and Evolution, 2014 doi: 10.1016/j.ympev.2014.02.015,IF=4.066)。
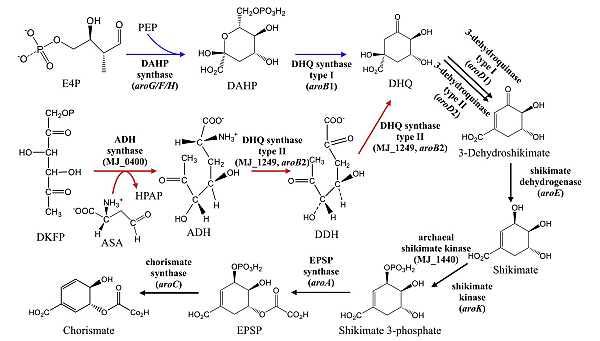
图1: 莽草酸通路示意图
关于甲基萘醌合成代谢通路起源和分子进化的研究发表在《基因组生物学与进化》(Genome Biology and Evolution,2014,61:149-160, IF=4.759)。1,4-dihydroxy-2-naphthoate是甲基萘醌极性头部,最初认为由原核微生物中的分支酸经过MK通路来合成。但最近的研究表明,在一些微生物中还存在着另外一条由MqnABCD和一些其它未知蛋白构成的通路(futalosine pathway)。虽然在现有的已测原核生物基因组中有32.1%的基因组含有经典的MK通路,只有13.3%的基因组含有futalosine通路,但是futalosine通路却有着更广泛的类群分布。同时结合对物种生境的研究,科研人员发现大多数含有经典MK通路的微生物生存在有氧或者兼性厌氧的环境中,而含有futalosine通路的物种则有着更加多样的生存环境。系统发育分析也表明,古菌和细菌之间经典MK通路的酶有很近的进化关系,它们可能起源于细菌的某个祖先,而非古菌和细菌的共同祖先。而来自futalosine通路的三个酶的系统发育结果表明,古菌和细菌之间的进化关系区分的相对清楚。根据这些结果,职晓阳博士等推断,futalosine通路可能比经典的MK通路有着更早的起源。

图2: 甲基萘醌合成代谢通路示意图
此外,汤森路透(Thomson Reuters)公司发布的Essential Science Indicators(基本科学指标,ESI)最新统计结果显示,云南大学微生物学科有2篇涉及放线菌新物种及放线菌分类体系更新的论文已进入2013年度全球前1%强,另有6篇论文进入全球前10%,1篇进入全球前20%。这些研究成果均出自云南大学放线菌资源与利用省级创新团队。
撰稿:祁志浩
(编辑:李哲)
我有话说
- 2021年全国职业院校技能大赛高职组工程测量赛项开幕式在我校隆重
初夏时节的春城昆明,万木向荣、生机勃发,昆明冶专校园里喜庆热烈,嘉宾云集、满园增辉。6月25日上午,由教育部......
- 2021年全国职业院校技能大赛高职组工程测量赛项闭幕式在我校成功
- 我校举办庆祝中国共产党成立100周年教职工演讲比赛
- 学校举行“光荣在党50年”纪念章颁发暨新发展党员宣誓大会
- 学校师生积极收看庆祝中国共产党成立100周年大会
- 学校举行庆祝中国共产党成立100周年暨学校”两优一先“表彰大会
- 王翠岗副书记专程为赴新疆就业毕业生送行
云中讯(通讯员李正良黄铮)7月8日上午8:00许,校党委副书记王翠岗率学工部、人文与管理学院负责同志前往昆明......
- 我校召开2013年科技工作座谈会
- 云南省健康教育协会中医专业委员会召开成立大会
- 我校召开党的群众路线教育实践活动动员大会
- 校党委召开理论学习中心组扩大会议
- 杨建军书记出席基础医学院2013届硕士研究生毕业典礼





